NAD Y NADP
Las coenzimas de nicotinamida
son nicotinamida adenina dinucleótido (NAD) y el fostato de nicotinamida
adenina dinucleótido (NADP), muy relacionado. Fueron ñas primeras coenzimas que
se conocieron. Ambas contienen nicotinamida, la amida del ácido nicotínico (figura 7.7). El ácido nicotínico (llamado también niacina) es el factor que
falta en la pelagra. Es esencial como precursor del NAFD Y NADP. (En muchas especies, el triptófano
se degrada a ácido nicotínico. En consecuencia, el triptófano en la dieta puede
suplir algo de los requisitos de niacina o nicotinamida). Como el ácido
nicotínico es el derivado de piridina con 3-carboxilo, con frecuencia se llama
coenzimas nucleótidos de piridina a las coenzimas de nicotinamida.
La asociación entre una
deshidrogenasa y el NAD o NADP es relativamente débil; el coenzima defiende
fácilmente desde un enzima a otro actúa como transportador de electrones
hidrosolubles desde un metabolismo a otro.
TABLA. Estereoespecificidad de
las deshidrogenasas que emplea NAD+ o NADP+
ENZIMA
|
COENZIMA
|
ESPECIFIDAD ESTEROQUIMICA PARA EL
ANILLO DE LA NICOTINAMIDA (A o B)
|
Isocitrato
deshidrogenasa
|
NAD+
|
A
|
α-cetoglutarato
deshidrogenasa
|
NAD+
|
B
|
Glucosa
6-fosfato deshidrogenasa
|
NADP+
|
B
|
malato
deshidrogenasa
|
NAD+
|
A
|
glutamato
deshidrogenasa
|
NAD+ o NADP+
|
B
|
gliceraldehído
3-fosfato deshidrogenasa
|
NAD+
|
B
|
lactato
deshidrogenasa
|
NAD+
|
A
|
alcohol
deshidrogenasa
|
NAD+
|
A
|
Las coenzimas de nicotinamida
participan en muchas reacciones de oxidación- reducción. Ayudan a la
trasferencias de electrones hacia metabolitos y desde estos. Las formas
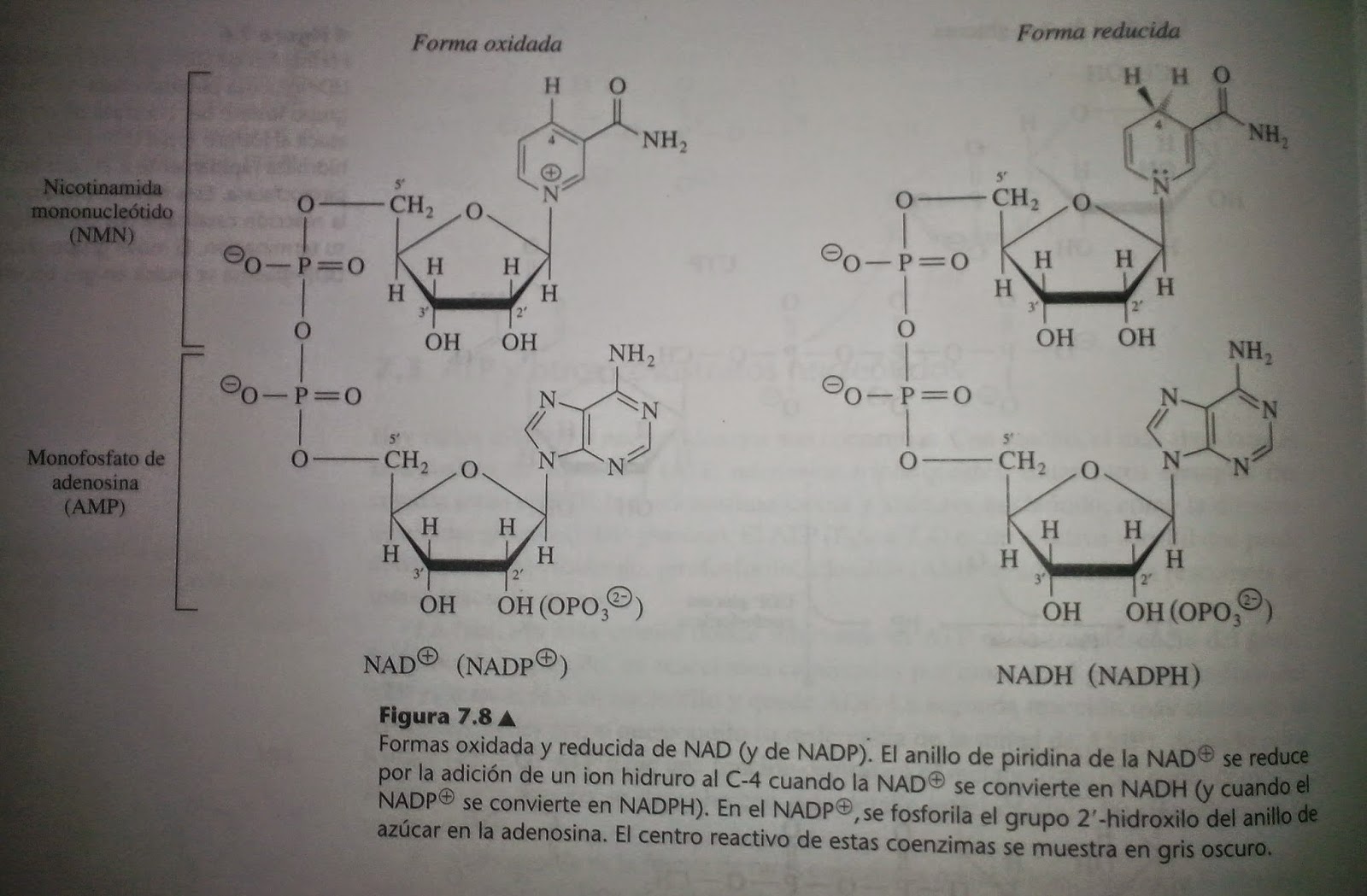
oxidadas, NAD y NADP, carecen de electrones, y las formas reducidas, NDDH y
NADPH, tienen un par adicional de electrones en forma de ion hidruro unido en
forma covalente. Las estructuras de estas coenzimas se ven en la figura 7.8.
Las dos coenzimas contienen un enlace fosfoanhídrido que une dos 5’-nucleotidos:
AMP y el robonucleótido de la nicitinamida, llamado nicotinamida monucleótido
(NMN) (formado aparte del ácido nicotínico).En
el caso del NADP, hay un grupo fosforilo en el átomo de oxígeno 2’ del
adenilato.
En la forma oxidada de la
coenzima (NAD Y NADP), al nitrógeno de la nicotinamida le falta uno de sus
electrones. Sólo tienen cuatro electrones en la capa externa, y están
compartidos con átomos adyacentes de carbono para formar un total de cuatro
enlaces covalentes. (Cada enlace tiene un par de electrones, de modo que la capa
externa del átomo de nitrógeno está llena con ocho electrones compartidos). Es
la causa de que la carga positiva se
asocie normalmente al átomo de nitrógeno del anillo, como se ve en la figura
7.8. De hecho, la carga está distribuida sobre todo el anillo aromático.
En particular, el átomo de
nitrógeno tiene cinco electrones en su capa externa. Dos de ellos En la forma
reducida, el anillo aromático tiene su complemento de electrones normal y
completo. (Representados con puntos en la figura 7.8). Son un par libre de electrones. Los tres
electrones participan en tres enlaces covalentes.
Casi siempre, el NAD y el NADP
actúan como consustratos para deshidrogenasas. Las deshidrogenasas dependientes
de nucleótidos de piridina catalizan la oxidación de sus sustratos,
transfiriendo dos electrones y un proton en forma de un ion hidruro (H) al C-4
del grupo nicotinamida del NADH o NADPH, donde se ha formado un nuevo enlace
C-H en el C-4 (un par de electrones) y el electrón que antes estaba asociado al doble
enlace del anillo se ha deslocalizado al átomo de nitrógeno del anillo. Así, la
oxidación por nucleótidos de piridina (o la reducción, la reacción inversa)
siempre se efectúa de dos en dos electrones.
Se dice que el NADH y el NADP,
que son estables en soluciones que contienen oxígeno, tiene poder reductor (es
decir, son reductores biológicos). La estabilidad de los nucleótidos de
piridina reducidos les permite llevar su poder reductor de una enzima a otra,
propiedad que no comparten las coenzimas derivadas de riboflavina.
La mayor parte de las reacciones que forman NADH Y NADPH son catabólicas. La
oxidación de NADH en las mitocondrias esta acoplada a la síntesis del ATP. La
mayor parte del NADPH se usa como agente reductor en reacciones de biosíntesis.
EL NADH Y EL FADH2 SON LOS PRINCIPALES TRANSPORTADORES DE ELECTRONES EN LA OXIDACIÓN DE MOLÉCULAS COMBUSTIBLES
El
nicotinamida adenina dinucleótido (NAD) es el principal aceptor de electrones
en la oxidación de las moléculas combustibles (fig. 17-7). La parte reactiva
del NAD es su anillo de nicotinamida.
Durante la oxidación de un sustrato, el anillo de nicotinamida del NAD acepta
un ion hidrogeno y dos electrones, lo que es equivalente a un ion hidruro. La
forma reducida de este transportador es el NADH.
En la forma oxidada, al átomo de nitrógeno es tetravalente y tiene una
carga positiva. En la forma reducida, NADH, el átomo de nitrógeno es
trivalente.
El
NAD es el aceptor de electrones de muchas reacciones del tipo.
En
esta deshidrogenación, un átomo de hidrogeno del sustrato se transfiere
directamente al NAD, mientras que el otro aparece en el otro disolvente, en
forma de protón. Los dos electrones perdidos por el sustrato se transfieren al
anillo de nicotinamida.
El
otro transportador electrónico importante
en la oxidación de los combustibles moleculares es el flavina adenina dinucleótido (fig.
17-8).
La
parte reactiva del FAD es el anillo de isoaloxazina (fig.17-9). El FAD, al
igual que el NAD, puede aceptar dos electrones. Al hacerlo, el FAD, a
diferencia del NAD, acepta un protón y un ion hidruro.







Hola, cual es tu referencia bibliográfica. Saludos
ResponderBorrarHola, cual es tu referencia bibliográfica. Saludos
ResponderBorrarMe puedes ayudar con la bibliografía
ResponderBorrar